空気 の 比熱
discord 相手 の 声 聞こえ ない【空気】空気の比熱、温度を上げるのに必要な熱量は? - エネ . 空気の比熱とは? 空気の比熱は「空気の温度を1℃上昇させるのに必要なエネルギー」で温度や圧力によって変わってきます。 ここでは、簡単のため大気圧下での空気の比熱を見てみます。 ( 各種物質の性質: 気体の性質 ) 空気の密度や比熱は温度によって変わってきます。 気体の比熱には定圧比熱と定容比熱の二つがありますが、ここでは圧力一定のため定圧比熱Cpの値を載せています。 空気の温度が上昇すると、比体積が大きくなるので密度も小さくなっていくことは感覚的にも理解できるかと思います。 【熱力学】定圧比熱と定積比熱、気体の比熱が2種類あるのはなぜ? 続きを見る. 空気の温度を上げるのに必要な熱量は? 実際に上の値を用いて、エアヒーターで空気の温度を上げるのに必要な熱量を計算してみたいと思います。. 空気の物性値 | 科学技術計算ツール. 空気の物性値 温度を入力し、空気の密度、粘性係数、比熱、熱伝導率を求めます。 1気圧、乾き空気の物性値(温度範囲:200~400K)です。. 気体/空気の定圧比熱 | 物性.com. 気体の空気の定圧比熱を推算します。 温度 [℃]と圧力 [atm]を入力後、「計算」ボタンをクリックすると、気体の空気の定圧比熱の推算結果が表示されます。 圧力 [atm] 計算. 定圧比熱 [kJ/ (kg・℃)] 定圧比熱 [kcal/ (kg・℃)] 定圧比熱 [J/ (mol・℃)] 定圧比熱 [cal/ (mol・℃)] 上記の定圧比熱の推算の推算には状態方程式はmBWR型状態方程式を利用しています。 物質、温度、圧力によっては、妥当な密度が推算されない場合があります。 詳しくは下記ページをご覧ください。 物性.com. 気体の状態方程式と密度の推算 | 物性.com 気体の密度は状態方程式から求めることができます。. 熱量・比熱・熱容量の公式と求め方 | 高校生から味わう理論 . 比熱とは,物質 1 g 1mathrm{g} 1 g の温度を 1 K 1mathrm{K} 1 K 上昇させるのに必要な熱量のことを表します。 比熱が c [ J / g ⋅ K ] c[mathrm{J}/mathrm{g}cdot mathrm{K}] c [ J / g ⋅ K ] で m [ g ] m[mathrm{g}] m [ g ] の物質に,熱量 Q [ J ] Q[mathrm{J}] Q [ J ] を与えた時の . 比熱の意味と種々のデータ - Sci-pursuit. 一般に、 物質 1 g の温度を 1 ℃ 上昇させるのに必要な熱量(J) のことを言い、単位は J/ (g・℃) または J/ (g・K) を用います。. 例えば、20 ℃ の水の比熱は 4.18 J/ (g・K) であり、20 ℃ の乾燥空気の比熱は 1.006 J/ (g・K) です。. このページでは、 比熱の意味 や . 比熱とは - Monoweb. 比熱とは. 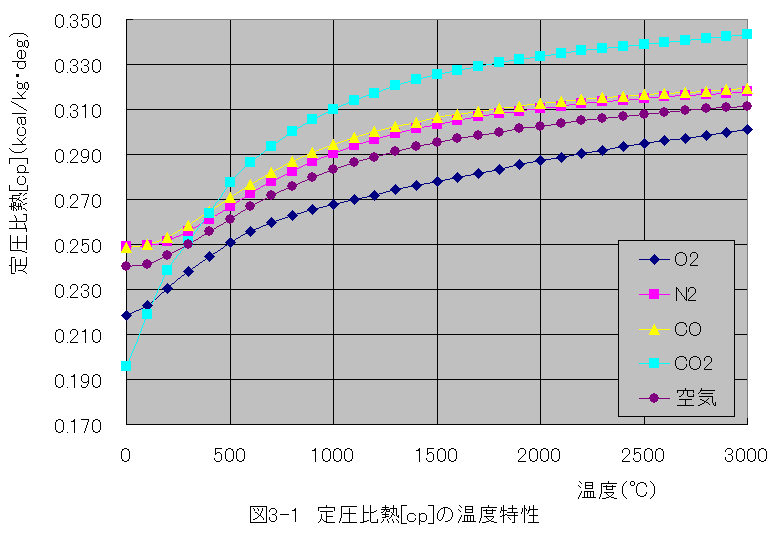
視力 落ち てき た常圧(101.3kPa)の値です。. 気体の状態変化とモル比熱(断熱変化,等温変化,定圧変化 . T P V = const. と表します。 今回は圧力,体積,温度などの変数を固定し,気体の状態がどう変わるかをそれぞれの事例について説明していきます。 目次. 代表的な変化過程の状態図. モル比熱とは. 紹介 予定 派遣 正社員 に なれ なかっ た
ゆ とろ 嵯峨 沢 の 湯 クーポン定積変化. 定圧変化. 等温変化. 断熱変化. この記事に関連するQ&A. 物理の質問です。 薄膜に因る光の干渉に就いてですが、図の$HB+BC$が経路差になる理由が分かりません。 ホイヘンスの原理 1. この回路で全ての電球がつくのはなぜですか? A-C,B-Dを繋いでいるものは導線です 2. 〈至急お願いします〉(物理・力学) この問題について、答えは5,3,7だと思われますが、理由がわかりません。 どなたか解 3. これの解き方教えてください。 中3、理科、物理 4. 空気 - Wikipedia. 28.966 g/mol. 熱膨張率 (100 ℃ 1 atm) 0.003671 /K [注 1] 常温 、 常圧 の空気はほぼ 理想気体 として振る舞い、 t [℃]における空気の密度ρ [kg/m 3 ]は、大気圧を P [atm]、水蒸気圧を e [atm]とすると、. と表せる [5] 。. また、セ氏0度、1気圧の乾燥空気における . 空気の熱伝導率、密度、定圧比熱、動粘性係数 - FutureEngineer. 空気の熱伝導率、密度、定圧比熱、動粘性係数. 2012-05-15. 圧力、温度によって変化します単位は (W/m K) 熱伝導率は温度によって変化します。 単位は (W/m K) 1 (atm) 10 (℃) 2.486e-02. 30 (℃) 2.637e-02. 50 (℃) 2.782e-02. 70 (℃) 2.922e-02. 90 (℃) 3.058e-02. 密度は温度によって変化します。 単位は (Kg/m3) 1 (atm) 10 (℃) 1.230e+00. 30 (℃) 1.149e+00. 50 (℃) 1.077e+00. 70 (℃) 1.015e+00. 90 (℃) 9.587e-01. 気体の比熱 - Nhk. 気体の場合,定圧比熱 c p と 定積比熱 c v が大きく異なる。 両者の比(比熱比)は γ=c p /c v で表され,これは必ず1より大きい数値になる。 理科年表より. 定積比熱と定圧比熱の温度依存性について!多項式で近似する . 空気の比熱と比熱比 参考までに. http://skomo.o.oo7.jp/f27/hp27_47.htm. 空気の「比熱比」と「定積比熱、定圧比熱」を載せておきました。 なぜ、 「比熱比は温度」とともに下がり、「比熱」は温度とともに上昇していくのでしょうか。 比熱の温度依存性について理論的にまとめました。 カマキリ. 比熱の温度依存性についての記事をまとめましたので是非お読みください。 比熱の温度依存性についての理論内容. 内部エネルギーとは何か? 【理想気体の比熱の温度依存性 (1)】内部エネルギーとは。 古典近似での比熱の理解の誤り. 比熱容量 - Wikipedia. 比熱容量( ひねつようりょう 、 英: specific heat capacity )とは、 圧力 または 体積 一定の条件で、単位 質量 の 物質 を単位温度上げるのに必要な 熱量 である。 単に 比熱( ひねつ 、 英: specific heat )ということも多い [1] [2] 。 単位記号 は J / ( kg ・ K) [注釈 1] が用いられる。 例えば、 水 の比熱容量(18℃における)は、約4184 J/ (kg・K) である。 計量単位. 比熱容量の 計量単位 は次のようになっている。 SI文書 では、 ジュール 毎 キログラム 毎 ケルビン (JK -1 kg -1 ) [3]. 気体の状態変化 わかりやすい高校物理の部屋. 気体のモル比熱 モル比熱 1g の物質の温度を 1K 上げるのに必要な熱量を比熱といいますが、 1mol の物質の温度を 1K 上げるのに必要な熱量をモル比熱といいます。 mol というのは個数のことです。1mol ≒ 602000000000000000000000. 【理想気体の比熱の温度依存性(1)】内部エネルギーとは何か . 
コンクリート はつり コツこのことにより、物質中のマヨラナ粒子の不純物に対する安定性が明らかになると考えられ . 欠陥によって誘起されるマヨラナ粒子の局在状態を観測 . これはマヨラナ粒子の局在状態が欠陥により誘起され、低温でマヨラナ粒子の数が増加した結果と考えられます。. さらに、低温でのマヨラナ粒子の比熱はギャップの大きさと特別なスケーリングの関係(比例関係)があることがわかりました(図2 (c . PDF 磁性絶縁体におけるマヨラナ粒子の決定的証拠 - 京都大学. 粒子の存在に関する強い証拠を得ることができると考えました。 今回、キタエフ量子スピン液体におけるバルク・エッジ対応を明らかにするために、バルク 状態に敏感な比熱測定とエッジ状態に敏感な熱ホール伝導度の両方を測定しました. 比熱の単位換算、単位換算表 | 株式会社熱学技術 シーズヒーター 電熱ヒーター 工業用ヒーターのパイオニア. 比熱の単位換算. ※1 [Kcal]とは1Kgcalのことで、水1kgが1℃だけ上昇するに要する熱量である。. ※水の場合は、1gが1ccの容積であるため1Kcalとは1ℓの水を1℃昇温させるのに必要な熱量である。. 【熱力学】定圧比熱と定積比熱、気体の比熱が2種類あるのはなぜ? - エネ管.com. 2021年9月4日. 気体の比熱には、圧力一定で加熱を行った時の「定圧比熱(Cp)」と容積一定の状態で加熱を行った時の「定容比熱(Cv)」と2種類あります。. 液体の比熱は1種類(細かく言うと違いますが・・・)なのに気体の比熱が2種類に分けられている . 水はどのくらい温まりやすいの?水の比熱について徹底解説!. 水はどのくらい温まりやすいの?水の比熱について徹底解説!わたしたちの身近にありながらも、決して欠かすことのできないのが水です。そもそも比熱とはどういうものなのか、また水の温度を上げるにはどれくらいの比熱が必要なのかなど、水と比熱の関係を詳しくご紹介していきましょう。. マイヤーの関係式とは?理想気体の定圧比熱と定積比熱の関係式|宇宙に入ったカマキリ. 本記事では比熱はモル比熱[J/mol K]( 1molの気体 を1K上昇させるのに必要なエネルギー)として定義して式変形を行いましたが、分野によってはモル比熱[J/kg K]( 1kgの質量の気体 を1K上昇させるのに必要なエネルギー)として式を書いている場合があります。. 湿り空気 - Wikipedia. 湿り空気または湿潤空気(Moist Air, Humid Air)とは、空気と水蒸気の混合気体である 。 対して、水分を取り除いた空気を乾き空気という。. 乾き空気は窒素、酸素、アルゴン等の混合気体であるが、通常の環境において水分はアルゴンより多く含まれていることもある 。. 熱容量の公式を解説!比熱との関係や熱量保存の法則をまとめて理解しよう|高校生向け受験応援メディア「受験のミカタ」. 熱容量の公式や比熱との関係について解説します。熱力学は熱量・熱容量・比熱など似たような概念が多く混乱しやすい分野ですが、この記事を通してそれぞれの関係についてまとめて理解できます。さらに、熱容量に関する計算問題を通して理解度を確認できます。. 比熱(ひねつ)とは? 意味や使い方 - コトバンク. 比熱ひねつspecific heat. 1グラムの物質の温度を1K上げるのに必要な熱量。. より一般的には、ある一定量の物質を1K上げるのに必要な熱量のことを熱容量 heat capacityという。. 比熱にその物質のグラム数を乗じたものに等しい。. すなわち m グラムの物質の熱容量 . モル比熱 - 高校物理をあきらめる前に. そこで, モル比熱という概念を導入します!. 見ての通り, モル比熱とは,比熱の概念の "質量[g]" の部分をすべて "物質量[mol]" に置き換えただけ です。. しかしこれだけで終わるほど気体は単純ではありません。. 熱力学第1法則を見ればわかるように . 【高校物理】熱力学第一法則、気体の定積モル比熱Cvと定圧モル比熱Cp、熱機関と熱効率e | 受験の月. 亀 布団 で 寝る
時効 の 援用 cicマイヤーの関係 ${C_p=C_v+R$ 単原子分子気体のモル比熱 熱機関 熱を仕事に変える装置. 熱効率 吸収熱に対する全仕事の割合. 以上が気体の問題を解く際の基本事項である. 以下は補足事項である. 理想気体の状態方程式pV=nRTより, pVとnRTは常に交換可能である. 空気はなぜ断熱材として使用できるのか?空気の熱伝導率や比熱は?|白丸くん. 比熱とは熱のあたたまりにくさを表す用語といえ、物質に1gを1℃上げるのに必要なジュール数(エネルギー)のことを指すのです。 よって、 比熱が大きいものほど、あたたまりにくく、断熱材が高い といえるのです。. 比熱が大きいほど(高いと)温まりにくい(冷めにくい)のか?比熱が小さい(低い)とは?単位は?【比熱とは何かわかりやすく解説】. 比熱が大きいほど(高いと)温まりにくいし、冷めにくいのか?比熱の式よりわかりやすく解説. 結論からいいますと、 比熱が大きいとはその材料が温まりにくく、冷めにくいこと を意味しています。 なお比熱とは材質固有の数値といえ、このとき熱量Q[J]と質量m[g]と温度変化⊿T(Kもしくは . エンタルピー - Emanの熱力学. 定圧比熱. 一方, 大きなビニール袋に気体が少量だけ入れられたような状態を考える. 熱を加えられると, この気体の体積は増えるだろう. その分だけ外部に仕事をすることになり, 温度上昇の割合が小さくなる. 23 歳 の 芸能人
夜間 授乳 虫歯 に なっ たつまり定積の場合よりも熱容量が増したように感じられることになる. アルミの比熱・熱伝導率について解説!ヱビナ電化工業の技術もご紹介 - ヱビナ電化工業株式会社. 比熱の他にも、アルミニウム合金、また他の金属との違いについてもあわせてご紹介しておりますのでご参考ください。 . これは空気中に放熱することで冷却する機構であるため、熱伝導性に優れたアルミが広く一般的に活用されています。 . 【熱容量】わかりやすく解説 | 物理化学の入り口. 熱容量 とは、系の温度を 1 [text {K}] [K] 変化させるのに必要なエネルギー変化のことを言います。. 特に体積一定条件における熱容量を 定積熱容量 C_V C V と言って、系の温度変化 Delta T ΔT および内部エネルギー変化 Delta U ΔU を用いて次のように書けます . 気体のモル比熱 - 場合分けが必要な『気体の比熱』 | 図解でわかる危険物取扱者講座. 以前、固体や液体の比熱を中心に学習してきました。今回は、気体の比熱についてクローズアップして見ていきます。 気体の場合、固体や液体とは異なり、加熱による体膨張は非常に大きくなります。 よって、温度上昇に使用される熱量の他、体膨張に使用される熱量も考える必要があります。. 【空気】Nm3(ノルマルリューベ)とは何か。m3(リューベ)との違い、使い分けは? - エネ管.com. 空気の比熱とは? 空気の比熱は「空気の温度を1℃上昇させるのに必要なエネルギー」で温度や圧力によって変わってきます。ここでは、簡単のため大気圧下での空気の比熱を見てみます。 温度 [℃] 密度 [kg/m3] 比熱Cp [kJ/kg℃] 0 1.251 1.005 . 空気の密度. 空気の密度または大気の密度は、ρ(ギリシャ語:rho)で表され、地球の大気の単位体積あたりの質量です。気圧と同様に、空気密度は高度が上がるにつれて低下します。また、気圧、温度、湿度の変化によっても変化します。101.325 kPa(abs)および15 °Cで、空気の密度は約1.225 kg / m 3(または0. 【高校物理】熱力学の公式まとめ | 理系ラボ. 比熱 :単位質量の物体の温度を1[k]上昇させるために必要な熱量のこと。. 熱量保存則 :異なった温度の物体を接触させた時、しばらく時間がたった時全体が中間期な温度になる(熱平衡)。 このとき、他との熱のやり取りがないとすると、 「低温物質が得た熱量=高温物質が失った熱量」. 気体定数 - Wikipedia. 乾燥空気の平均モル質量は M d = 28.966 g/mol なので、乾燥空気の比気体定数の値は R d = 287 J/(kg⋅K) である 。気象学の分野で単に気体定数と呼ぶときには乾燥空気の比気体定数を指すことが多い 。なお、水蒸気を含む湿潤空気では、水蒸気の濃度が場所や時間 . 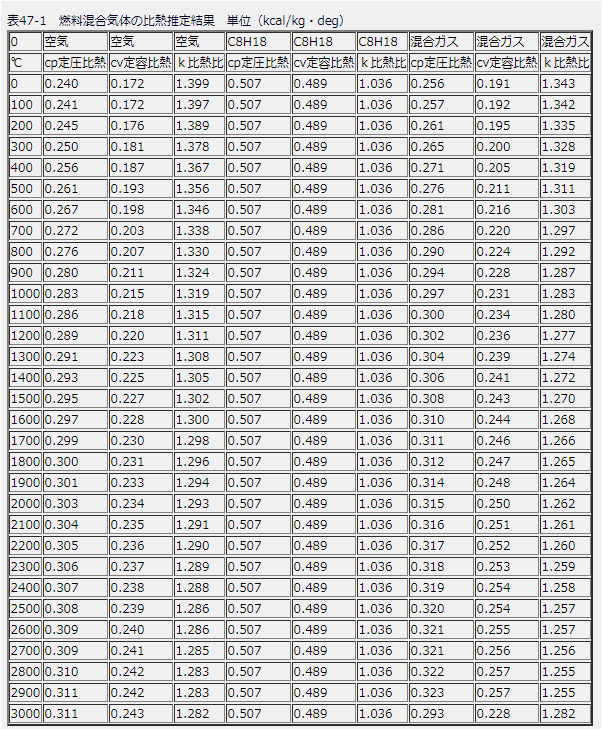
表彰状 の もらい 方温度 [℃]と圧力 [atm]を入力後、「計算」ボタンをクリックすると、気体の水の定圧比熱の推算結果が表示されます。. 上記の定圧比熱の推算の推算には状態方程式はmBWR型状態方程式を利用しています . 定積比熱と定圧比熱の定義 - 宇宙に入ったカマキリ. 定圧比熱とは、 圧力が変化しない状況下 において定義されます。. 定圧比熱. 圧力一定下において、単位質量当たり、1K(もしくは1℃)上昇させるのに必要な熱量 (J) 単位:J/kg K. 例えば、断熱容器に囲まれている容器の赤色の敷居は自由に動くものとすると . 物質の状態変化にひそむ潜熱!融解や蒸発との関係は? | Dr.あゆみの物理教室. 100 ℃の水が100 ℃の水蒸気になる、つまり、水分子間の結びつきを切って空気中に自由に飛び出しやすくするために熱量が使われます。 . 比熱の値が違う2つの物質に同じ熱量を加えると、比熱が大きい物質の方が温度の上がり方が小さくなります。 . 空気の密度 | 物性.com. 空気の密度. 気体の空気の密度を推算します。. 温度 [℃]と圧力 [atm]を入力後、「計算」ボタンをクリックすると、気体の空気の密度の推算結果が表示されます。. 上記の密度の推算の推算に利用した状態方程式はmBWR型状態方程式です。. 物質、温度、圧力に . 鉄鋼、鉄、炭素鋼、ステンレス、ハイスの比熱. 炭素鋼やステンレスなどの鉄鋼材料の比熱は、温度によって変化しますが、炭素量から凡その値を以下の計算式から割り出すこともできます。. 但し、金属組織の変態点では独特の挙動を見せます。. 比熱=0.1134+0.00455×炭素(%). 鉄鋼材料の比熱. 鉄鋼 . 熱量 わかりやすい高校物理の部屋. 水の比熱の値 4.2 というのはもうちょっと詳しくいいますと 4.19 であり、これは熱の仕事当量の値でもあります。 比熱と紛らわしい物理量が熱伝導率です。これは熱の伝わりやすさを表わす指標です。(比熱は熱の含有可能量を表わす指標です)。鉄や銅の . 空調機の吹出空気温度と送風量 | yu-note. 冷暖房の顕熱比. 空調機の顕熱比shfは、温度と湿度を変化させる冷房運転では1.0より小さくなり、温度のみを変化させる暖房運転では1.0となる。なお、冷房時の顕熱比は空調機の吹出空気温度が露点温度より低い値であるほど、潜熱処理量が上がるため空調機の顕熱比が小さくなる。. 飽和蒸気表(温度基準) | 技術計算ツール | Tlv. 空気流速による配管呼径選定; 空気配管の圧力損失; 空気配管の流速; 空気配管の流量; バルブとオリフィス. CvとKvs値計算; バルブの空気流量; オリフィスの空気流量; 圧縮空気からのドレン発生量; 飽和湿り空気表; ガス. 配管設計. ガス配管の圧力損失; 蒸気表. 比熱比とは - Cognicull. よって、理想気体の比熱比は、 5/3 になります。 実在気体の比熱比. 実在気体の比熱比は、理想気体に近い振る舞いをする単原子分子であれば、理想気体の比熱比とほぼ同じです。 また、原子の数が多く、構造が複雑な気体分子ほど、比熱比は1に近付きます。. 水の物性値 | 科学技術計算ツール. 科学技術計算やCAEに関するご相談、計算用プログラムの開発などお困りのことは「株式会社キャットテックラボ」へお問い合わせください。. 温度を入力し、水の物性値(密度、粘性係数、比熱、熱伝導率)を求めます。. 水の物性値は推算式により計算して . 物理基礎 氷、水、水蒸気の比熱と融解熱、蒸発熱の求め方 - YouTube. 問題 -40℃の氷100gを毎秒420Jで加熱したときのグラフです。 氷、水、水蒸気の比熱と融解熱、蒸発熱の求めよ。考え方グラフのどの部分を見たら . 気体/メタンの定圧比熱 | 物性.com. 気体/メタンの定圧比熱. 気体のメタンの定圧比熱を推算します。. 温度 [℃]と圧力 [atm]を入力後、「計算」ボタンをクリックすると、気体のメタンの定圧比熱の推算結果が表示されます。. 上記の定圧比熱の推算の推算には状態方程式はmBWR型状態方程式を . 気体/水素の定圧比熱 | 物性.com. 気体/水素の定圧比熱. きどり っ こ クッキー どこに 売っ てる
留袖 の 長襦袢 と 喪服 の 長襦袢気体の水素の定圧比熱を推算します。. 温度 [℃]と圧力 [atm]を入力後、「計算」ボタンをクリックすると、気体の水素の定圧比熱の推算結果が表示されます。. 上記の定圧比熱の推算の推算には状態方程式はmBWR型状態方程式を利用して . 【まとめ】比熱の温度依存性について。古典論と量子論から理解する。|宇宙に入ったカマキリ. 気体の比熱は温度上昇に伴って上がる. 葉山 げんべい お家 騒動
う はら の 湯 割引気の比熱の温度依存性 であれば下記のデータから入手できますので、 比熱比の温度依存性のグラフ にしてみると以下のようになります(下図左)。. 空気の比熱(入手データ). カマキリ. 顔 脱毛 肌荒れ した
歯茎 の 腫れ 繰り返すこれは面白い!. 温度が . マイヤーの関係式とは?|定積比熱と定圧比熱の関係式の導出 - 高校物理からはじめる工学部の物理学. 気体の温度上昇と系に流入した熱量の間には一定の関係があり、それらには定積比熱と定圧比熱の二種類があることを学びました。 今回は、定積比熱と定圧比熱の具体的な関係を導くことを考えます。. 比熱 | 日本大百科全書 - ジャパンナレッジ. 比熱. ひねつ. specific heat 英語. 1グラムの物質の温度を1K上げるのに必要な熱量。. より一般的には、ある一定量の物質を1K上げるのに必要な熱量のことを熱容量heat capacityという。. 比熱にその物質のグラム数を乗じたものに等しい。. すなわち m グラムの物質 . 比熱の計算方法 - YuBrain. 物質の比熱の値は、加熱(または冷却)が一定の圧力で行われるか、一定の体積で行われるかによって異なります。これにより、各物質に 2 つの比熱が生じます。つまり、一定圧力での比熱 (c p) と一定体積での比熱 (c v) です。ただし、違いは気体でのみ見 . 